Декомпенсация хронической сердечной недостаточности(ХСН) с потребностью во внутривенном введении мочегонных является самой частой причиной госпитализации этой категории пациентов. Возможным решением проблемы является разработка лекарственных форм мочегонных, которые обладали бы действием, близким к в/в диуретикам, но могли бы использоваться амбулаторно без посторонней помощи. Два года назад FDA зарегистрировало лекарственную форму фуросемида для подкожного введения, которая соответствует по фармакокинетике и фармакодинамике в/в форме фуросемида. Помимо препарата, коммерческий продукт Furoscix (scPharmaceuticals) включает в себя одноразовую систему доставки препарата (см рисунок), которая прикрепляется к передней брюшной стенке. Инфузия препарата в дозе 80 мг осуществляется в течение 4 часов. Лечение не показано в экстренных ситуациях или у пациентов с острым отеком легких, а также не предназначено для постоянного использования вместо пероральных диуретиков.
В журнале JACC: Heart Failure опубликованы результаты пилотного исследования 2 фазы AT HOME-HF, в котором подкожное введение фуросемида сравнивается со стандартной тактикой у амбулаторных пациентов с прогрессированием застоя.
В группу подкожного введения включено 34 пациента, в группу стандартной тактики – 17 пациентов.
В исследовании не удалось продемонстрировать преимуществ по первичной конечной точке (иерархическая сумма неблагоприятных событий – сердечно-сосудистой смерти, событий, связанных с ухудшением ХСН, и динамики NT-proBNP). Однако подкожное введение фуросемида ассоциировалось с большим уменьшением массы тела (рассматривался в качестве маркера выраженности застоя): на 3-и сутки различия между группами составили -2.02 кг (95% ДИ от −3.9 до −0.14; P = 0.035). Также существенные различия были выявлены по индексу одышки к 7-м суткам (P = 0.017), а также по динамике теста с 6-минутной ходьбой (P = 0.032). Отмечалась тенденция к улучшению качества жизни, объективизированного по результатам Канзасского опросника.
Самый частый побочный эффект в группе подкожного введения фуросемида – легкая боль в месте введения (регистрировалась у 11,8% участников).
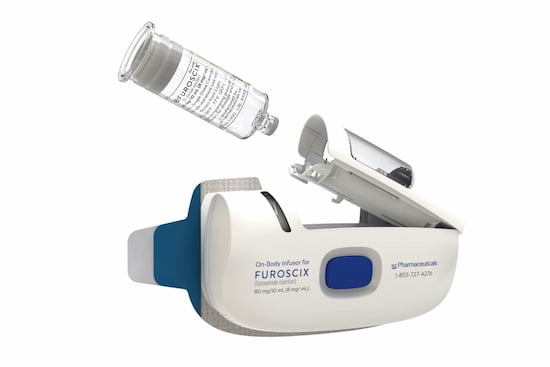
Рисунок (источник: www.furoscix.com)
По материалам:
J Am Coll Cardiol HF. Sep 11, 2024. Epublished DOI: 10.1016/j.jchf.2024.07.015
